您现在的位置是: 首页 > 教育改革 教育改革
2019浙江省高考化学,2019浙江高考化学
tamoadmin 2024-06-27 人已围观
简介1.浙江高考用的全国几卷2.2019年高考理综分数是怎样分配的3.2019年四平市高考状元,四平市高考状元分数名单和学校 专项4-温度条件的控制 一.升高温度 1.促进某些离子的水解,如高价金属阳离子,易水解的阴离子 练习1目前世界上新建的金矿中约有80%都采用氧化法提金。某工厂利用锌冶炼渣
1.浙江高考用的全国几卷
2.2019年高考理综分数是怎样分配的
3.2019年四平市高考状元,四平市高考状元分数名单和学校
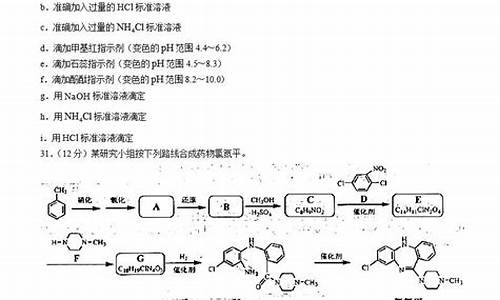
专项4-温度条件的控制
一.升高温度
1.促进某些离子的水解,如高价金属阳离子,易水解的阴离子
练习1目前世界上新建的金矿中约有80%都采用氧化法提金。某工厂利用锌冶炼渣回收金、银等贵金属的流程如下图所示:
已知HCN有剧毒,其Ka(HCN)=5×10-10,Au++2CN-=[Au(CN)2]-平衡常数KB=1×1038
“氰化”环节中,金的溶解速率在80℃时达到最大值,但生产中控制反应液的温度在10-20℃,原因是:___________________________(答一点即可)。
答案温度的升高,促进了氰化物的水解,增加了HCN的挥发速度;温度的升高,Ca(OH)2的溶解度减小,部分碱从溶液中析出。
?
练习2某化工厂“用含NiO的废料(杂质为Fe2O3、?CaO、?CuO等)制备羟基氧化镍(2NiOOH·H2O)的工艺流程如图:
如图是酸浸时镍的浸出率与温度的关系,则酸浸时合适的浸出温度是____________℃,若酸浸时将温度控制在80℃左右,则滤渣1中会含有一定量的Ni(OH)2,其原因可能是_________________________。
答案70 ?随着温度的升高,Ni2+水解程度增大,从而形成一定量的Ni(OH)2沉淀
解析由图可知当温度在70°左右时镍的浸出率较高,故酸浸时适宜的温度为70°C;Ni2+能水解,生成Ni(OH)2,升温能促进水解,所以80℃左右滤渣1中会含有一定量的Ni(OH)2。
练习3氯化亚铜是一种重要的化工产品,常用作有机合成催化剂,还可用于颜料、防腐等工业,它不溶于H2SO4、HNO3和醇,微溶于水,可溶于浓盐酸和氨水,在潮湿空气中易水解氧化成绿色的碱式氯化铜[Cu2(OH)3Cl]。以海绵铜(主要成分是Cu和少量CuO)为原料,采用硝酸铵氧化分解技术生产CuCl的工艺过程如下:
(1)析出的CuCl晶体水洗后要立即用无水乙醇洗涤,在真空干燥机内于70℃干燥2h,冷却密封包装。70℃真空干燥、密封包装的原因是____________________________________________________________。
(2)如图是各反应物在最佳配比条件下,反应温度对CuCl产率影响.由图可知,溶液温度控制在60℃时,CuCl产率能达到94%,当温度高于65℃时,CuCl产率会下降,其原因可能是______________________________________________________________________________________________。
答案(1)真空干燥可以加快乙醇和水的挥发,密封包装可以防止CuCl在潮湿空气中水解、氧化;
(2)因在60℃时CuCl产率最大,根据信息可知,随温度升高,促进了CuCl的水解,CuCl被氧化的速度加快。
练习4TiO2·xH2O沉淀与双氧水、氨水反应40min所得实验结果如下表所示:
温度/℃
30
35
40
45
50
TiO2·xH2O转化率
92
95
97
93
88
分析40℃时TiO2·xH2O转化率最高的原因_____________________。
答案40℃时TiO2?xH2O转化率最高,因低于40℃,TiO2?xH2O转化反应速率随温度升高而增加,超过40℃,双氧水分解与氨气逸出导致TiO2?xH2O转化反应速率下降
解析40℃时TiO2?xH2O转化率最高,因低于40℃,TiO2?xH2O转化反应速率随温度升高而增加,超过40℃,双氧水分解与氨气逸出导致TiO2?xH2O转化反应速率下降。
?
2.促进平衡向吸热方向移动
练习1二硫化钼是重要的固体润滑剂,被誉为“高级固体润滑油之王”。利用低品相的辉钼矿(含MoS2、SiO2以及CuFeS2等杂质)制备高纯二硫化钼的一种生产工艺如图:
(4)由图分析可知产生MoS3沉淀的流程中选择的最优温度和时间是___________,利用化学平衡原理分析低于或高于最优温度时,MoS3的产率均下降的原因_______________________________________。
(5)利用低品相的原料制备高纯产品是工业生产中的普遍原则。如图所示,反应[Ni(s)+4CO(g)
答案(4)40℃、30min ?温度太低,反应MoS42-+2H+
解析(4)根据图象可知,40℃、30min MoS3沉淀率达到最大,所以最优温度和时间是40℃、30min;温度太低,反应MoS42-+2H+
(5)[Ni(s)+4CO(g)
?
3.加快反应速率或溶解速率
2020新课标Ⅰ钒具有广泛用途。黏土钒矿中,钒以+3、+4、+5价的化合物存在,还包括钾、镁的铝硅酸盐,以及SiO2、Fe3O4。采用以下工艺流程可由黏土钒矿制备NH4VO3。
“酸浸氧化”需要加热,其原因是_________________________________________。
答案加快酸浸和氧化反应速率(促进氧化完全)
解析“酸浸氧化”需要加热,其原因是:升高温度,加快酸浸和氧化反应速率(促进氧化完全),故答案为:加快酸浸和氧化反应速率(促进氧化完全);
(1)研究温度对“降解”过程中有机物去除率的影响,实验在如图1所示的装置中进行。
①在不同温度下反应相同时间,发现温度从60℃升高到95℃时,有机物去除率从29%增大到58%,其可能的原因是:MnO2的氧化能力随温度升高而增强;______________________________________。
答案温度升高,反应速率加快
解析①升高温度,反应速率加快,在相同时间内有机物反应的更多,去除率增加。
练习3“浸取”步骤中,能加快浸取速率的方法有___________(任写两种)。
答案将橄榄石尾矿粉碎、适当增大盐酸的浓度、适当提高反应的温度等
解析“浸取”步骤中,能加快浸取速率的方法有将橄榄石尾矿粉碎、适当增大盐酸的浓度、适当提高反应的温度等。
?
4.使沸点相对低的原料气化,或者降低在溶液中的气体溶解度
练习1实验室用如图所示的装置模拟燃煤烟气脱硫实验:
研究发现石灰石浆液的脱硫效率受pH和温度的影响。燃煤烟气流速一定时,脱硫效率与石灰石浆液pH的关系如图所示,在pH为5.6时脱硫效果最佳,石灰石浆液
答案石灰石的溶解度减小,与
解析由脱硫效率与石灰石浆液pH的关系图知,在pH为5.6时脱硫效果最佳,pH增大,石灰石的溶解度减小,与
练习2以甲酸和碳酸钾为原料生产二甲酸钾,实验测得反应条件对产品回收率的影响如下:
表1 反应温度对产品回收率的影响
反应温度(℃)
20
30
40
50
60
70
80
产品回收率(%)
75.6
78.4
80.6
82.6
83.1
82.1
73.7
②实际生产二甲酸钾时应选择的最佳反应条件是反应温度应控制在____________℃~____________℃,由表1可知反应温度过高,反应回收率反而会降低,其原因可能是___________________________________________。
答案温度过高,甲酸挥发
解析从表1可看出,温度控制在50℃~60℃二甲酸钾的产率较高,温度过高,反应回收率反而会降低,其原因可能是:甲酸易挥发,温度太高甲酸挥发了。
练习3实验室中用FeSO4溶液与NaOH溶液制备Fe(OH)2,装置如图,请回答下列问题:
配制NaOH溶液时使用的蒸馏水通常要煮沸,其目的是__________________________________。
答案除去水中溶解的氧气
解析硫酸亚铁易被氧化而变质,因此配制NaOH溶液时,应排除溶液中的氧气,可用加热溶液的方法除去溶解的氧气。
练习4四氯化锡用作媒染剂和有机合成上的氯化催化剂,实验室制备四氯化锡的反应、装置示意图和有关信息数据如下:
②无水四氯化锡是无色易流动的液体,熔点-33℃,沸点114.1℃。
实验制得的SnCl4中因溶解了C12而略显**,提纯SnCl4的方法是________________。
答案加热蒸馏
解析由于SnCl4的沸点114.1℃,因此如果实验制得的SnCl4中因溶解了C12而略显**,提纯SnCl4的方法是加热蒸馏。
练习5白云石的主要成份是CaCO3·MgCO3,在我国有大量的分布。以白云石为原料生产的钙镁系列产品有广泛的用途。白云石经煅烧、熔化后得到钙镁的氢氧化物,再经过碳化实现Ca2+、Mg2+的分离。碳化反应是放热反应,化学方程式如下:Ca(OH)2+Mg(OH)2+3CO2
碳化温度保持在50~60℃。温度偏高不利于碳化反应,原因是__________________、__________________。温度偏低也不利于碳化反应,原因是___________________________。
答案二氧化碳的溶解度小;碳酸氢镁分解,反应速率较小。
解析该反应为放热反应,而且是可逆的,当温度过高时,平衡逆反应方向移动,二氧化碳的溶解度减小,导致钙镁离子的分离减弱,Mg(HCO3)2是易分解,温度过高就分解了,温度过低,反应速率太小,导致得到产物消耗的时间太长,不利于碳化反应,故答案为:二氧化碳的溶解度小、碳酸氢镁分解;反应速率较小。
?
5.除去热不稳定的杂质,如NH 4 HCO 3 、NH4(CO 3 ) 2 、 KMnO 4 、NH 4 C1等物质
练习1物质的分离与提纯是化学的重点,请根据下列实验目的,分别选择相应的操作和实验装置。下列为操作:
a.蒸馏 ?b.结晶法 ?c.加适量水,过滤 ?d.加热(或灼烧) ?e.加适量盐酸,蒸发 ?f.萃取分液 ?g.分液 h.升华
下列为实验装置:
(1)除去氯化钠晶体中的碳酸钠:______、______(分别填操作序号及实验装置图编号,下同)。
(2)除去碳酸钙中的氯化钠:_______、______。
(3)分离乙酸(沸点118℃)和乙酸乙酯(沸点77.1℃)的混合液(两者互溶):______、______。
(4)从溴水中提取溴:_______、_______。
(5)除去氧化钙中的碳酸钙:_______、_______。
(6)分离固体食盐和碘的方法:_______、_______。
答案e ?2 ?c ?1 ?a ?5 ?f ?4 ?d ?3 ?h ?6 ?
解析
(1)碳酸钠与盐酸反应生成NaCl,则加适量盐酸,蒸发可分离,对应于装置2,故答案为e;2;
(2)碳酸钙不溶于水,氯化钠晶体溶于水,则选择过滤法可分离,对应于装置1,故答案为c;1;
(3)二者互溶,但沸点不同,则选择蒸馏法分离,对应于装置5,故答案为a;5;
(4)溴不易溶于水,易溶于有机溶剂,则选择萃取、分液法分离,对应于装置4,故答案为f;4;
(5)碳酸钙高温分解生成氧化钙,则选择加热分解法除杂,对应于装置3,故答案为d;3;
(6)碘容易升华,则选择升华法分离固体食盐和碘,对应于装置6,故答案为h;6。
?
二.降低温度
1.防止某物质在高温时会分解(或溶解)
练习1电解精炼铜的阳极泥中主要含Ag、Au等贵重金属。以下是从精炼铜的阳极泥中回收银、金的流程图:
铜阳极泥氧化时,采用“低温焙烧”而不采用“高温焙烧”的原因是_______?______________。
答案低温焙烧时,Ag与氧气转化为Ag2O,高温时,氧化银分解又生成Ag和氧气;故答案为:高温焙烧时,生成的Ag2O又分解为Ag和O2(或2Ag2O
练习22018北京卷磷精矿湿法制备磷酸的一种工艺流程如下:
已知:磷精矿主要成分为Ca5(PO4)3(OH),还含有Ca5(PO4)3F和有机碳等。溶解度:Ca5(PO4)3(OH)<CaSO4·0.5H2O
(1)H2O2将粗磷酸中的有机碳氧化为CO2脱除,同时自身也会发生分解。相同投料比、相同反应时间,不同温度下的有机碳脱除率如图所示。80℃后脱除率变化的原因:____________________。
答案图示是相同投料比、相同反应时间,不同温度下的有机碳脱除率,80℃前温度升高反应速率加快,相同
练习3一种从铜阳极泥(主要含有铜、银、金、少量的镍)中分离提取多种金属元素的工艺流程如下:
“分铜”时,如果反应温度过高,会有明显的放出气体现象,原因是____________________________。
答案温度过高,H2O2分解放出氧气。
练习5钛铁矿主要成分为FeTiO3(含有少量MgO、SiO2等杂质),Li4Ti5O12和LiFePO4都是锂离子电池的电极材料,可利用钛铁矿来制备,工艺流程如下:
过程②中固体TiO2与双氧水、氨水反应转化成(NH4)2Ti5O15溶液时,Ti元素的浸出率与反应温度的关系如图2所示,反应温度过高时,Ti元素浸出率下降的原因是___________________________________________________。
答案温度过高,双氧水分解与氨气逸出导致Ti元素浸出率下降。
练习6工业上以软锰矿(主要成分是MnO2,含有SiO2、Fe2O3等少量杂质)为主要原料制备高性能的磁性材料碳酸锰(MnCO3)。其工业流程如下:
(1)“浸锰”反应中往往有副产物MnS2O6生成,温度对“浸锰”反应的影响如右图所示,为减少 MnS2O6 的生成,“浸锰”的适宜温度是___________________________。
(2)向过滤Ⅱ所得的滤液中加入NH4HCO3 溶液时温度控制在30-35℃,温度不宜太高的原因是___________________________________________________________________。
答案(1)90℃。(2)铵盐受热分解,向过滤所得的滤液中加入碳酸氢铵溶液,温度控制在30-35℃的原因是防止NH4HCO3受热分解,提高原料的利用率;
?
2.使化学平衡向着放热方向移动
练习1乙酸苯酚酯制备: 将
①用碎冰块代替水可能的原因是:______________________________________ .
答案该反应是放热反应,碎冰温度低有利于酯的生成
解析①碎冰温度低有利于酯的生成,故答案为:该反应是放热反应,碎冰温度低有利于酯的生成。
?
3.使某个沸点高的产物液化,使其与其他物质分离
练习1石墨在材料领域有重要应用。某初级石墨中含SiO2(7.8%)、Al2O3(5.1%)、Fe2O3(3.1%)和MgO(0.5%)等杂质。设计的提纯和综合应用流程如下:
(注:SiCl4的沸点是57.6?C,金属氯化物的沸点均高于150?C)
向反应器中通入Cl2前,需通一段时间的N2。高温反应后,石墨中的氧化物杂质均转变为相应氯化物。80℃冷凝的目的是:_____________________。②由活性炭得到气体Ⅱ的化学反应方程式为:_____________________。
答案高温下,Si元素转化成SiCl4,铁元素转化成FeCl3,Mg元素转化成MgCl2,Al元素转化成AlCl3,SiCl4沸点是57.6℃,MgCl2、FeCl3、AlCl3沸点均高于150℃,加热到1500℃,MgCl2、FeCl3、AlCl3、SiCl4全部转化成气体I,80℃冷凝,SiCl4还是气体,而MgCl2、FeCl3、AlCl3状态是固体,便于与SiCl4分开。
?
4.降低晶体的溶解度,减少损失。
练习1碳酸锂广泛应用于化工、冶金等行业.工业上利用锂辉石(Li2Al2Si4Ox)制备碳酸锂的流程如图:
已知:碳酸锂的溶解度为(g/L)
温度
0
10
20
30
40
50
60
80
100
Li2CO3
1. 54
1. 43
1. 33
1. 25
1. 17
1. 08
1. 01
0. 85
0. 72
(1)硫酸化焙烧温度控制在250℃﹣300℃之间,主要原因是__________________________________;焙烧中硫酸用量控制在理论用量的l15%左右,硫酸加入过多的副作用是_________________________。
(2)“沉锂”需要在95℃以上进行,主要原因是_______________________,过滤碳酸锂所得母液中主要含有硫酸钠,还可能含有_____________和______________。
答案(1)硫酸化焙烧温度控制在250℃﹣300℃之间,主要原因是温度低于250℃,反应速率较慢,温度高于300℃,硫酸挥发较多;焙烧中硫酸用量控制在理论用量的l15%左右,硫酸加入过多的副作用是后续中还需要除去过量的硫酸,增加后续杂质的处理量、增加后续中和酸的负担。
(2)温度越高,碳酸锂溶解度降低,减少碳酸锂溶解,可以增加产率;溶液中硫酸钠不反应,使用碳酸钠要过量,少量碳酸锂溶解在溶液中,过滤碳酸锂所得母液中主要含有硫酸钠,还可能含有碳酸钠和碳酸锂。过滤碳酸锂所得母液中主要含有硫酸钠,还可能含有碳酸钠和碳酸锂。所以“沉锂”需要在95℃以上进行,主要原因是温度越高,碳酸锂溶解度降低,可以增加产率;过滤碳酸锂所得母液中主要含有硫酸钠,还可能含有碳酸钠和碳酸锂。
练习2某废旧电池材料的主要成分为钴酸锂(LiCoO2),还含有一定量的铁、铝、铜等元素的化合物,其回收工艺如图所示,最终可得到Co2O3和锂盐。
已知:CoC2O4·2H2O微溶于水,它的溶解度随温度升高而逐渐增大,且能与过量的C2O42-离子生成Co(C2O4)n2(n-1)-而溶解。
(4)“沉钴”过程中,(NH4)2C2O4的加入量(图a)、沉淀反应的温度(图b)与钴的沉淀率关系如图所示:
①随n(C2O42-):N(Co2+)比值的增加,钴的沉淀率先逐渐增大后又逐渐减小的原因________________________。
②沉淀反应时间为10 min,温度在50℃以上时,随温度升高而钴的沉淀率下降的可能原因是_______________________________________________________________________________________________。
答案①过量的C2O42-与Co2+反应生成Co(C2O4)n2(n-1)-而溶解 ?②它的溶解度随温度升高而逐渐增大 ?
解析①随n(C2O42-):N(Co2+)比值的增加,过量的C2O42-与Co2+反应生成Co(C2O4)n2(n-1)-而溶解,钴的沉淀率先逐渐增大后又逐渐减小;
②沉淀反应时间为10 min,温度在50℃以上时,溶解度随温度升高而逐渐增大。
?
5.减少能源成本,降低对设备的要求
练习1目前常用的工业生产纯碱的方法是“联合制碱法(侯氏制碱法)”
世界上最早工业生产碳酸钠的方法是“路布兰法”,其流程如下:
与“路布兰法”相比,“联合制碱法’的优点之一是_________________________。
答案原料利用率高,反应所需温度低,耗能少 ?
解析据流程可知:路布兰法是利用食盐晶体和浓硫酸在600°C到700°C下反应生成硫酸钠和氯化氢,再利用C与石灰石和硫酸钠在1000°C生成碳酸钠;侯德榜研究出联合制碱法为在饱和的氯化钠溶液中直接通入氨气和CO2,得到氯化铵和碳酸氢钠晶体,并利用碳酸氢钠的分解制得纯碱,
?
?
三.控制温度(用水浴或油浴控温)
1 . 防止某种物质温度过高时会分解或挥发
2019江苏实验室以工业废渣(主要含CaSO4·2H2O,还含少量SiO2、Al2O3、Fe2O3)为原料制取轻质CaCO3和(NH4)2SO4晶体,其实验流程如下:
(1)废渣浸取在如图所示的装置中进行。控制反应温度在60~70 ℃,搅拌,反应3小时。温度过高将会导致CaSO4的转化率下降,其原因是?;保持温度、反应时间、反应物和溶剂的量不变,实验中提高CaSO4转化率的操作有?。
答案由于铵盐具有不稳定性,受热易分解,所以温度过高,(NH4)2CO3分解,从而使CaSO4转化率下降;由于浸取过程中的反应属于固体与溶液的反应(或发生沉淀的转化),保持温度、反应时间、反应物和溶剂的量不变,提高CaSO4转化率即提高反应速率,结合外界条件对化学反应速率的影响,实验过程中提高CaSO4转化率的操作为加快搅拌速率(即增大接触面积,加快反应速率,提高浸取率)。
?
2 . 控制固体的溶解与结晶
习题12017新课标3卷重铬酸钾是一种重要的化工原料,一般由铬铁矿制备,铬铁矿的主要成分为FeO·Cr2O3,还含有硅、铝等杂质。制备流程如图所示:
有关物质的溶解度如图所示。向“滤液3”中加
浙江高考用的全国几卷
浙江省2019年高考理综总分平均分估计是230。今年理综的化学题目比较新颖,但是并没有脱离考纲,都是换汤不换药的试题,考生只要平时复习到位,脑子稍微灵活一点,拿分是比较容易的。很多考生表示,模拟考试时候从来没做过这么有意思的题目,希望可以再考一遍,看来,今年的化学试题是深得人心了。而对于物理题目,选择题部分也是非常基础简单,但是,后面的两道答题则是一如既往的难。不管怎样,高考已经结束,考生现在要调整心态。
2019年高考理综分数是怎样分配的
浙江高考不用全国卷,是浙江省自主命题。浙江是新高考改革试点地区,全部高考科目均是自主命题。
2019年浙江高考全部科目均自主命题,一切都是遵照高考大纲命题。高考自主命题即是各个省份可以不使用教育部编写的全国试卷,单独组织本省教师进行考试试卷的编写,即自主进行高考试卷的单独命题。
浙江高考改革政策解读
①不分文理;
②除语数外,再从物理、化学、生物、政治、历史、地理、技术7门中选3门进行选考计入高考总分;
③外语和选考科目有两次考试机会,成绩两年有效;
④语数外每门150分,选考科目分等级打分,每门最高100分,总分750分;
⑤取消一二本等批次区别。
2019年四平市高考状元,四平市高考状元分数名单和学校
高考理综的总分数为300分,其中物理分数为110分,化学分数为100分,生物分数为90分。在高考考试时答理综卷要掌握一定的答题方法。
考试时间150分钟,全卷难度值0.6左右(其中物理:0.55~0.60,化学:0.60~0.65,生物:0.60~0.65)。理科综合试卷满分300分,其中物理120分,选考内容占10%。
化学100分,选考内容占13%。生物80分,选考内容约占12%。其中理综每个单选选择题是6分,物理的多选选择题也是6分。
高考理综考试与单科考试有很大的不同,理、化、生在同一张试卷上,要知道在高考中时间的安排是否合理对你成败有着十分关键的作用。
对于高考理综非选择题答题时要认真审题、分清楚问题的来龙去脉这样才能够给出正确答案。这样保证高考理综考试取得一个很高的分数。
四平市高考状元,四平市高考状元分数名单和学校
1、四平市高考状元上课专注,不懂就问,刨根问底
不管是语文、数学这样的主科课,还是生物、化学副科课,课堂上的许东都倾注了百分之百的专注度,班主任王荷描述许东:“他的眼睛,会跟老师对话。”而遇到不懂的问题,他绝不会得过且过,一定会在第一时间跳出来跟老师“争论”。他十分看重解题思路,比如英语的学习,对于英语阅读中的选择题,大部分学生在了解答案后就直接背下来,而许东则是常常追究其解答的思路,并且带领整个班级养成一种刨根问底的氛围。
2、四平市高考状元按时作息,高效学习
谈到作息,许东每天晚上九点三刻准时上床睡觉,从不玩题海战术,不打疲劳战,他很注重课堂的学习,认为只有充足的休息,才能保证白天课堂上集中精力听讲。同时,许东注重学习效率的提高,他常常是周五放学就能把作业写好,而别的学生可能周末还在埋头于题海之中。
3、四平市高考状元兴趣广泛、多面发展
许东有一点和很多高考状元不一样的地方,便是在忙碌的高中就开始投入不少时间发展自己的兴趣爱好。他从小喜欢看动漫、喜欢打游戏,从初中开始自学日语。高一结束后,许东考过了日语一级,并且加入了网络上火爆的“翻译组”,高中3年时间,一共翻译了50多万字的日语小说。许东还喜欢计算机编程,利用业余时间自学各类编程语言。课外时间还会在网络上找到许多志同道合的小伙伴,一起开发网络游戏。不仅如此,为了培养艺术修养,许东还从初中开始学习架子鼓。即便高中学业紧张的时候,也几乎没有放弃。做题累了就敲上一个小时,既是休息也能修身养性。
4、四平市高考状元看历届考题,从盲点攻克
何雨轩是个主张轻松学习的人,该学时就认真对待,该放松时绝不沾染一丝和学习有关的事情。向来不认为“学霸”就是那是埋头苦学的代名词。学习绝对不可以“死”学,题海战术不可避免,但不能盲目做题,而要根据自己对题型的“盲点”去攻克。对照历届高考考试热点知识,找出自己的盲点去做题,会事半功倍。
5、四平市高考状元养成良好学习习惯,脚踏实地
高考是场持久战,何雨轩从上高中的第一天起,就已经开始认真对待每一天。他认为,培养良好的学习习惯,保持固定的学习规律是首要的,其次,还要脚踏实地的去对待每一道题,会就会,不会就不会,绝不马虎应付,绝不蒙蔽自己。
6、四平市高考状元认真听课很重要
翟颖佳认为,她成绩好的秘诀就是对学习有兴趣,上课的时候认真听,她从不会在课堂上做一些其他的事情,有些同学时不时开下小差,很有可能就错过了一些老师讲的重要知识点。
7、四平市高考状元每天都要保持题型练习
翟颖佳说自己不会用题海战术,但会每天保持各个题型都要做几道练习,她认为做够一定的题量能帮助自己找到答题的感觉。虽然她是文科生,但因为文科数学和理科数学略有差异,所有每次考完试,她还会去借理科的试题,自己研究一遍,
8、四平市高考状元学习文科要掌握主要框架
对于学习文科的成功经验,翟颖佳认为不仅仅是简单的背诵,而是掌握知识的主框架和体系,依附主干添枝加叶,答题过程中多总结答案的模型,经过一些模仿练习就会拿到高分。
北京市高考理科状元刘智昕来自人大附中的高三(5)班的刘智昕以721分拿下北京市高考理科状元语文136,数学145,英语147,理综293总分721分。生于1998年1月8日的她如今刚刚17岁,一副乖乖女模样丝毫想不到她是超级大学霸。
北京今年文科状元蔡雨玹今年北京市高考文科状元花落 北京师范大学 第二附属中学(以下简称师大二附),高三九班的蔡雨玹以699分夺得北京高考文科第一名,其中语文142分,数学150分,英语135分,文综272分。
今年上海理科状元许东我是“学霸”做啥像啥高考分数:557分(语文:123分,数学:149分,外语:138分,化学:147分)
今年上海文科状元刘逸冲从典型理科男转型文科“学霸”高考成绩:526分(语文112分、数学147分、英语140分、政治127分)
天津今年高考理科状元大港油田实验中学赵秋阳获得今年天津市高考理科状元!总成绩706分。大港油田实验中学高三理科班高考成绩语文133分数学143分外语140分理综290分总分706分
天津今年高考文科状元耀华中学张杨子苏获得今年天津市高考文科状元!总成绩684分。耀华中学高三文科班高考成绩语文132分数学142分外语145分文综265分总分684分
今年江苏高考理科状元花落泰州姜堰区泰州姜堰中学高三(8)班蒋婧煜以总分425分的高分荣获全省理科状元。
今年江苏高考文科状元花落南通南通中学高三(11)班袁清晗同学以418分成为江苏文科状元。今年山东高考理科状元出自山东嘉祥一中。山东嘉祥一中贾晶同学以726分裸分加5分省级三好学生加分,总分731分成为山东理科状元。
今年山东高考文科两位状元分别出自山东青州市第一中学和山东胶州市第一中学。山东青州市第一中学陈兰君同学和山东省胶州市第一中学向淑婷同学以681分裸分并列成为山东文科状元。
四川理科第一名是绵阳中学高三13班高志华,以总分689分的成绩夺得。
四川省文科第一名是成都外国语学校学生万妙然(如图女孩),考分681分
湖北今年高考理科状元襄阳五中刘世豪,699分。各科成绩分别为语文126,数学141,英语146,理综286。
湖北今年高考文科状元襄阳五中陈凤竹,3分。
今年广西高考文理科状元文科状元柳铁一中凌志宇以672分摘取今年广西省文科状元(上图男孩)。今年广西高考理科状元为全州高中李忠明,以总分721摘取今年广西省理科状元。
今年宁夏理科状元是银川一中何雨轩,以691分的成绩夺得宁夏理科状元。
今年宁夏文科状元是银川二中高三(A)班马悦,以662分的实分获得今年宁夏高考[微博]文科状元,以682分的虚分获得宁夏今年高考第一名!据说数学考了满分。
今年江西高考理科第一名为江西师大附中考生夏子哲,总分715分。
今年江西高考文科第一名是江西师大附中考生虞筱隽和婺源天佑中学考生朱攀,并列文科第一名,总分同为637分。
今年浙江高考理科状元郑恩柏浙江文、理科第一名都出自镇海中学。理科第一名:郑恩柏(男)760分(语文132分,数学144分,英语142分,理综282分,自选模块60分)。
今年浙江高考文科状元严丹华745分
今年吉林省高考理科状元来自吉林油田高中的李明煜以708分获得吉林省高考理科状元桂冠
今年吉林省高考文科状元吉大附中的王爽与张哲以661分的成绩并列第一名。
今年内蒙古高考理科裸分状元平煤高中杨正宇同学以698分获今年高考内蒙理科裸分状元,续写了2000-今年16年连出内蒙古赤峰市23名高考状元的佳绩。
今年内蒙古高考文科状元朱宇昕同学以裸分654分的成绩获得内蒙古自治区文科状元。
今年甘肃高考理科状元来自民乐一中的王复英以总分676分摘取理科第一名桂冠。
今年甘肃省高考文科状元惠雅婕来自西北师大附中,总分660分。
今年重庆高考理科状元是南开中学学生张瑞伽以719分强势夺得
今年重庆高考文科状元刘楠枫总分704分,其中数学150、英语146、文综279
今年河北高考理科加分状元是河北唐山一中刘泽群,728分,其中加分20分。语文:135分;数学:150分;英语:143分;理综:280分;总分:708分
今年河北高考理科裸分状元保定满城中学的史旭同学,语文:128分;数学:147分;英语:144分;理综:298分;总分:717分
今年河北高考文科状元被石家庄二中南校区的张皓辰同学摘得,语文:132分;数学:143分;英语:143分;文综:257分;总分:675分
今年海南省高考理科状元最高分考生为海南中学高三一班何声楷同学,900分。
今年海南省高考文科状元最高分考生为海南中学高三二十班孙笑涵同学,894分。
今年黑龙江高考理科状元为来自大庆实验中学的魏毓良,他取得了708分的好成绩,
今年黑龙江高考文科状元哈三中南岗校区张集森则以661分夺得文科状元。其中语文129分,数学145分,外语139分,综合248分。
今年辽宁高考理科状元抚顺二中高三一班的李昀格以裸分709分荣获今年高考辽宁省理科状元
今年辽宁高考文科状元盘锦市高级中学的戴霖杉以666分获得辽宁高考文科状元!
今年贵州高考理科状元常青、向佳旋两名同学以695分并列全省理科状元
今年贵州高考文科状元兴义八中学生马欢以714分的成绩勇夺全省文科状元
今年云南省高考理科状元出自曲靖一中。该校理19班刘德斌以实考分725分夺得高考理科状元。
今年云南省高考文科状元出自曲靖一中。文20班朱俊瑞以实考分691分夺得高考文科状元。
今年安徽高考理科状元最高分708分,两人。其中,“理科状元”来自马鞍山二中和合肥八中,马鞍山二中“状元”叫冯沁雪
今年安徽高考理科状元来自合肥八中的“状元”叫吴苾婵,最高分708分
今年安徽高考文科状元来自蚌埠二中,叫赵昕玥总分689分
今年福建高考理科状元厦门英才学校姜麟锟!总分703分!语文128分,数学145分,英语139分,理综291分
今年福建高考文科状元连江一中学生丁若泓,文科663分,获全省文科第一
今年河南省高考理科状元全省理科第一名考生为祝乐,男毕业学校:太康一高北清三班成绩:704分
今年河南省高考文科状元全省文科第一名考生为胡瑞环,男毕业学校:扶沟县高级中学高三(39)班成绩:638分(裸分)
今年山西高考理科状元来自山西运城市新绛县海泉中学,应届生1208班王江珊,成绩686分
今年山西高考文科状元来自山西大学附属中学考生翟颖佳以627分的成绩名列全省文科考生榜首。
今年陕西高考理科第一名霍柳蓉18岁的霍柳蓉觉得自己并非完美主义者,但在今年的高考中她交出了一份完美的答卷:数学150分(满分)、英语146分、理综293分、语文140分,总分729分,获得了陕西省理科第一名
今年陕西高考文科第一名孙轶群西工大附中高三文科二班的孙轶群总分658分
今年湖南高考理科状元湖南师大附中孙嘉玮同学高考718分,获得湖南省今年理科状元。
今年湖南高考文科状元桑植一中的顾殊涵以档案分680的成绩摘得湖南今年高考文科桂冠